Molekyylibiologian teknologian jatkuvan kehityksen myötä geenimutaatioiden ja vikojen ja sairauksien välinen suhde on saanut yhä syvempää ymmärrystä.Nukleiinihapot ovat herättäneet paljon huomiota, koska niillä on suuri käyttöpotentiaali sairauksien diagnosoinnissa ja hoidossa.Nukleiinihappolääkkeet viittaavat keinotekoisesti syntetisoituihin DNA- tai RNA-fragmentteihin, joilla on sairauden hoitotoimintoja.Tällaiset lääkkeet voivat vaikuttaa suoraan sairautta aiheuttaviin kohdegeeneihin tai tautia aiheuttaviin kohde-mRNA:ihin ja niillä on rooli sairauksien hoidossa geenitasolla.Verrattuna perinteisiin pienimolekyylisiin lääkkeisiin ja vasta-ainelääkkeisiin, nukleiinihappolääkkeet voivat säädellä sairauksia aiheuttavien geenien ilmentymistä juurista alkaen, ja niillä on "oireiden hoitamisen ja perimmäisen syyn parantamisen" ominaisuuksia.Nukleiinihappolääkkeillä on myös ilmeisiä etuja, kuten korkea tehokkuus, alhainen toksisuus ja korkea spesifisyys.Sen jälkeen kun ensimmäinen nukleiinihappolääke fomivirseninatrium lanseerattiin vuonna 1998, monet nukleiinihappolääkkeet on hyväksytty kliiniseen hoitoon.
Tällä hetkellä maailmanlaajuisesti markkinoilla olevia nukleiinihappolääkkeitä ovat pääasiassa antisense-nukleiinihappo (ASO), pieni häiritsevä RNA (siRNA) ja nukleiinihappoaptameerit.Nukleiinihappoaptameerejä (jotka voivat ylittää 30 nukleotidia) lukuun ottamatta nukleiinihappolääkkeet ovat yleensä oligonukleotideja, jotka koostuvat 12-30 nukleotidista, jotka tunnetaan myös oligonukleotidilääkkeinä.Lisäksi miRNA:t, ribotsyymit ja deoksiribotsyymit ovat osoittaneet suurta kehitysarvoa erilaisten sairauksien hoidossa.Nukleiinihappolääkkeistä on tullut yksi lupaavimmista biolääketieteen tutkimuksen ja kehityksen aloista nykyään.
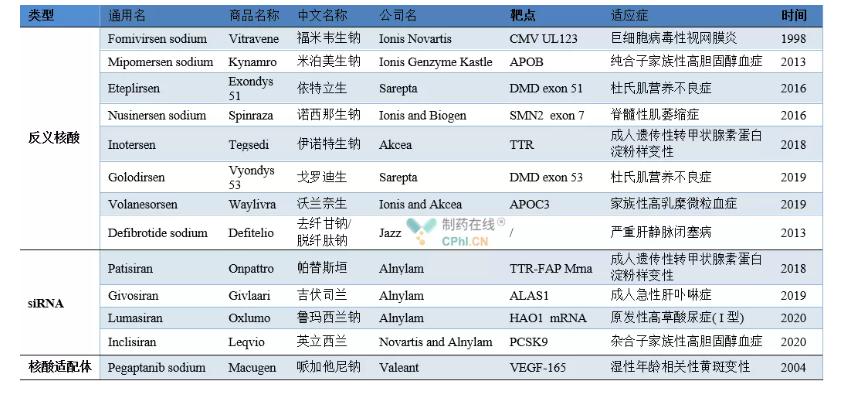
Esimerkkejä hyväksytyistä nukleiinihappolääkkeistä
Antisense-nukleiinihappo
Antisense-teknologia on uusi lääkekehitysteknologia, joka perustuu Watson-Crick-emäksen komplementaatioperiaatteeseen ja jossa käytetään spesifisiä komplementaarisia DNA- tai RNA-fragmentteja, jotka organismi on syntetisoinut tai syntetisoinut keinotekoisesti säätelemään spesifisesti kohdegeenien ilmentymistä.Antisense-nukleiinihapolla on kohde-RNA:lle komplementaarinen emässekvenssi ja se voi sitoutua spesifisesti siihen.Antisense-nukleiinihapot sisältävät yleensä antisense-DNA:n, antisense-RNA:n ja ribotsyymit.Niiden joukossa antisense-DNA:n korkean stabiilisuuden ja alhaisten kustannusten ominaisuuksien vuoksi antisense-DNA:lla on hallitseva asema antisense-nukleiinihappolääkkeiden nykyisessä tutkimuksessa ja käytössä.
Fomivirsen-natriumin (kauppanimi Vitravene) on kehittänyt Ionis Novartis.Elokuussa 1998 FDA hyväksyi sen sytomegaloviruksen aiheuttaman retiniitin hoitoon immuunipuutteisilla potilailla (pääasiassa AIDS-potilailla), ja siitä tuli ensimmäinen markkinoille tuotu nukleiinihappolääke.Fomivirseeni estää CMV:n osittaista proteiiniekspressiota sitoutumalla spesifiseen mRNA:han (IE2) ja säätelee siten virusgeenien ilmentymistä terapeuttisten vaikutusten saavuttamiseksi.Potilasmääriä huomattavasti vähentäneen tehokkaan antiretroviraalisen hoidon ilmaantumisen vuoksi Novartis kuitenkin peruutti vuonna 2002 ja 2006 Fomivirsen-lääkkeiden myyntiluvan Euroopassa ja Yhdysvalloissa, ja tuote on jäädytetty markkinoilta.
Mipomersen-natrium (kauppanimi Kynamro) on ranskalaisen Genzymen kehittämä ASO-lääke.Tammikuussa 2013 FDA hyväksyi sen homotsygoottisen familiaalisen hyperkolesterolemian hoitoon.Mipomersen estää ApoB-100 proteiinin (apolipoproteiinin) ilmentymistä sitoutumalla ApoB-100mRNA:han, mikä vähentää merkittävästi ihmisen matalatiheyksisten lipoproteiinien kolesterolia, matalatiheyksisiä lipoproteiinia ja muita indikaattoreita, mutta sivuvaikutusten, kuten maksatoksisuuden vuoksi, 13.12.2012 hylättiin myös EMA hakemus myyntiin.
Syyskuussa 2016 FDA hyväksyi Sareptan kehittämän Eteplirsenin (kauppanimi Exon 51) Duchennen lihasdystrofian (DMD) hoitoon.DMD-potilaat eivät voi normaalisti ekspressoida toiminnallista antiatrofista proteiinia kehon DMD-geenin mutaatioiden vuoksi.Eteplirsen sitoutuu spesifisesti proteiinin pre-lähetti-RNA:n (Pre-mRNA) eksoniin 51, poistaa eksonin 51 ja palauttaa joitain alavirran geenejä. Normaali ilmentyminen, transkriptio ja translaatio dystrofiinin osan saamiseksi terapeuttisen vaikutuksen saavuttamiseksi.
Nusinersen on Spinrazan kehittämä ASO-lääke spinaalisen lihasatrofian hoitoon, ja FDA hyväksyi sen 23. joulukuuta 2016. Vuonna 2018 FDA hyväksyi Tegsedin kehittämän Inotesenin aikuisten perinnöllisen transtyretiiniamyloidoosin hoitoon.Vuonna 2019 FDA hyväksyi Golodirsenin, jonka Sarepta on kehittänyt Duchennen lihasdystrofian hoitoon.Sillä on sama vaikutusmekanismi kuin Eteplirsenillä, ja sen vaikutuspaikasta tulee eksoni 53. Samana vuonna Ionisand Akcean yhdessä kehittämä familiaalisen hyperkylomikronemian hoitoon kehittämä Volanesorsen hyväksyi Euroopan lääkeviraston (EMA).Volanesorsen säätelee triglyseridien aineenvaihduntaa estämällä apolipoproteiini C-Ⅲ:n tuotantoa, mutta sillä on myös sivuvaikutuksena verihiutaleiden tasoa alentava vaikutus.
Defibrotidi on Jazzin kehittämä oligonukleotidiseos, jolla on plasmiiniominaisuuksia.Se sisältää 90 % yksijuosteista DNA:ta ja 10 % kaksijuosteista DNA:ta.EMA hyväksyi sen vuonna 2013, ja sen jälkeen FDA hyväksyi sen vaikeiden maksalaskimojen hoitoon.Okklusiivinen sairaus.Defibrotidi voi lisätä plasmiinin aktiivisuutta, lisätä plasminogeeniaktivaattoria, edistää trombomoduliinin noususäätelyä ja vähentää von Willebrand -tekijän ja plasminogeeniaktivaattorin estäjien ilmentymistä terapeuttisten vaikutusten saavuttamiseksi.
siRNA
siRNA on pieni RNA-fragmentti, jolla on tietty pituus ja sekvenssi, joka on tuotettu leikkaamalla kohde-RNA.Nämä siRNA:t voivat spesifisesti indusoida kohde-mRNA:n hajoamisen ja saavuttaa geenin vaimentavia vaikutuksia.Verrattuna kemiallisiin pienimolekyylisiin lääkkeisiin siRNA-lääkkeiden geeniä vaimentavalla vaikutuksella on korkea spesifisyys ja tehokkuus.
11. elokuuta 2018 ensimmäinen siRNA-lääke patisiran (kauppanimi Onpattro) hyväksyttiin FDA:ssa ja lanseerattiin virallisesti.Tämä on yksi tärkeimmistä virstanpylväistä RNA-häiriöteknologian kehityshistoriassa.Patisiranin kehittivät yhdessä Alnylam ja Genzyme, Sanofin tytäryhtiö.Se on siRNA-lääke perinnöllisen tyroksiinivälitteisen amyloidoosin hoitoon.Vuonna 2019 FDA hyväksyi givosiranin (kauppanimi Givlaari) toiseksi siRNA-lääkkeeksi aikuisten akuutin maksaporfyrian hoitoon.Vuonna 2020 Alnylam kehitti ensisijaisen tyypin I lääkkeen lasten ja aikuisten hoitoon.FDA hyväksyi lumasiranin, jolla on korkea oksaluria.Joulukuussa 2020 EMA hyväksyi Inclisiranin, jonka Novartis ja Alnylam ovat kehittäneet aikuisten hyperkolesterolemian tai sekamuotoisen dyslipidemian hoitoon.
Aptamer
Nukleiinihappoaptameerit ovat oligonukleotideja, jotka voivat sitoutua useisiin kohdemolekyyleihin, kuten pieniin orgaanisiin molekyyleihin, DNA:han, RNA:han, polypeptideihin tai proteiineihin suurella affiniteetilla ja spesifisyydellä.Vasta-aineisiin verrattuna nukleiinihappoaptameereillä on yksinkertaisen synteesin ominaisuudet, alhaisemmat kustannukset ja laaja valikoima kohteita, ja niillä on laajempi potentiaali lääkkeiden käyttöön sairauksien diagnosoinnissa, hoidossa ja ehkäisyssä.
Pegaptanibi on ensimmäinen nukleiinihappoaptameerilääke, jonka Valeant on kehittänyt kostean ikääntymiseen liittyvän silmänpohjan rappeuman hoitoon, ja FDA hyväksyi sen vuonna 2004. Sen jälkeen EMA ja PMDA hyväksyivät sen tammikuussa 2006 ja heinäkuussa 2008, ja se tuli markkinoille.Pegaptanibi estää angiogeneesiä spatiaalisen rakenteen ja verisuonten endoteelin kasvutekijän yhdistelmällä terapeuttisten vaikutusten saavuttamiseksi.Sen jälkeen se on kohdannut kilpailua vastaavien lääkkeiden Lucentis kanssa, ja sen markkinaosuus on pudonnut paljon.
Nukleiinihappolääkkeistä on muodostunut kuuma paikka kliinisten lääke- ja uusien lääkeaineiden markkinoilla niiden merkittävän parantavan vaikutuksen ja lyhyen kehityssyklin ansiosta.Nousevana huumeena se kohtaa haasteita samalla kun se kohtaa mahdollisuuksia.Sen eksogeenisten ominaisuuksien vuoksi nukleiinihappojen spesifisyydestä, stabiilisuudesta ja tehokkaasta kuljetuksesta on tullut pääkriteerit arvioitaessa, voivatko oligonukleotidit tulla erittäin tehokkaiksi nukleiinihappolääkkeiksi.Kohteen ulkopuoliset vaikutukset ovat aina olleet nukleiinihappolääkkeiden avainkohta, jota ei voida jättää huomiotta.Nukleiinihappolääkkeet voivat kuitenkin vaikuttaa taudin aiheuttavien geenien ilmentymiseen juuresta alkaen ja saavuttaa sekvenssispesifisyyden yhden emäksen tasolla, jolla on "perussyyn ja oireiden hoitamisen" ominaisuuksia.Yhä useampien sairauksien vaihtelevuuden vuoksi vain geneettisellä hoidolla voidaan saavuttaa pysyviä tuloksia.Muihin liittyvien teknologioiden jatkuvan parantamisen, täydellisyyden ja edistymisen myötä nukleiinihappolääkkeet, joita edustavat antisense-nukleiinihapot, siRNA ja nukleiinihappoaptameerit, käynnistävät varmasti uuden aallon sairauksien hoidossa ja lääketeollisuudessa.
Rviittaukset:
[1] Liu Shaojin, Feng Xuejiao, Wang Junshu, Xiao Zhengqiang, Cheng Pingsheng.Nukleiinihappolääkkeiden markkina-analyysi maassani ja vastatoimet[J].Chinese Journal of Biological Engineering, 2021, 41(07): 99-109.
[2] Chen Wenfei, Wu Fuhua, Zhang Zhirong, Sun Xun.Tutkimuksen edistyminen markkinoitavien nukleiinihappolääkkeiden farmakologiassa[J].Chinese Journal of Pharmaceuticals, 2020, 51(12): 1487-1496.
[3] Wang Jun, Wang Lan, Lu Jiazhen, Huang Zhen.Markkinoitujen nukleiinihappolääkkeiden tehon ja tutkimuksen edistymisen analyysi[J].Chinese Journal of New Drugs, 2019, 28(18): 2217-2224.
Tietoja kirjoittajasta: Sha Luo, kiinalaisen lääketieteen tutkimus- ja kehitystyöntekijä, työskentelee tällä hetkellä suuressa kotimaisessa lääketutkimus- ja kehitysyhtiössä ja on sitoutunut uusien kiinalaisten lääkkeiden tutkimukseen ja kehittämiseen.
Liittyvät tuotteet:
Postitusaika: 19.11.2021