1. Perustiedot (jos haluat nähdä kokeellisen osan, siirrä suoraan toiseen osaan)
Perinteisen PCR:n johdannaisreaktiona reaaliaikainen PCR valvoo pääasiassa amplifikaatiotuotteen määrän muutosta jokaisessa PCR-amplifikaatioreaktion syklissä reaaliajassa fluoresenssisignaalin muutoksen kautta ja analysoi kvantitatiivisesti aloitustemplaattia ct-arvon ja standardikäyrän välisen suhteen kautta.
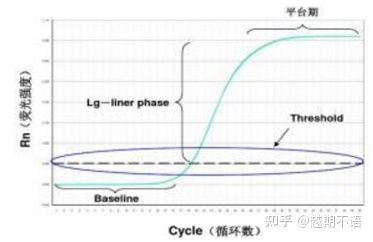
RT-PCR:n erityistiedot ovatperusviiva, fluoresenssin kynnysjaCt arvo.
| perusviiva: | Jakson 3-15 fluoresenssiarvo on perusviiva (perusviiva), joka johtuu mittauksen satunnaisesta virheestä. |
| Kynnys (kynnys): | Viittaa fluoresenssin havaitsemisrajaan, joka on asetettu sopivaan kohtaan monistuskäyrän eksponentiaalisella kasvualueella, yleensä 10 kertaa perusviivan standardipoikkeama. |
| CT-arvo: | Se on PCR-syklien lukumäärä, jolloin kunkin reaktioputken fluoresenssiarvo saavuttaa kynnyksen. Ct-arvo on kääntäen verrannollinen alkuperäisen mallin määrään. |
Yleiset leimausmenetelmät RT-PCR:lle:
| menetelmä | etu | puute | soveltamisala |
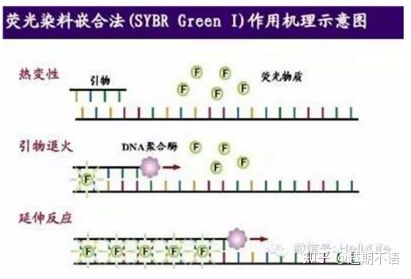
| SYBR VihreäⅠ | Laaja sovellettavuus, herkkä, halpa ja kätevä | Pohjusteen vaatimukset ovat korkeat, alttiita epäspesifisille vyöhykkeille | Se soveltuu erilaisten kohdegeenien kvantitatiiviseen analysointiin, geeniekspression tutkimukseen sekä siirtogeenisten rekombinanttieläinten ja -kasvien tutkimukseen. |
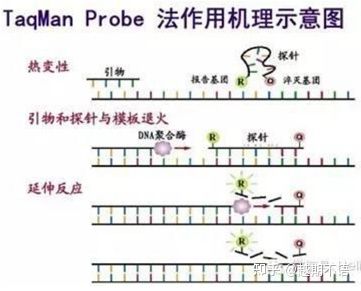
| TaqMan | Hyvä spesifisyys ja hyvä toistettavuus | Hinta on korkea ja sopii vain tiettyihin tavoitteisiin. | Patogeenien havaitseminen, lääkeresistenssigeenitutkimus, lääketehon arviointi, geneettisten sairauksien diagnosointi. |
| molekyylimajakka | Korkea spesifisyys, fluoresenssi, matala tausta | Hinta on korkea, se sopii vain tiettyyn tarkoitukseen, suunnittelu on vaikeaa ja hinta on korkea. | Spesifinen geenianalyysi, SNP-analyysi |
2. Kokeiluvaiheet
2.1 Tietoja kokeellisesta ryhmittelystä- ryhmässä on oltava useita kuoppia, ja niissä on oltava biologisia toistoja.
| ① | Tyhjä ohjaus | Käytetään solujen kasvutilan havaitsemiseen kokeissa |
| ② | Negatiivinen kontrolli siRNA (epäspesifinen siRNA-sekvenssi) | Osoita RNAi:n toiminnan spesifisyys.siRNA voi indusoida epäspesifisen stressivasteen pitoisuudella 200 nM. |
| ③ | Transfektioreagenssikontrolli | Sulje pois transfektioreagenssin toksisuus soluille tai vaikutus kohdegeenin ilmentymiseen |
| ④ | siRNA kohdegeeniä vastaan | Tukahduttaa kohdegeenin ilmentyminen |
| ⑤ (valinnainen) | positiivinen siRNA | Käytetään kokeellisten järjestelmien ja toimintaongelmien vianmäärityksessä |
| ⑥ (valinnainen) | Fluoresoiva kontrolli siRNA | Solutransfektion tehokkuutta voidaan tarkkailla mikroskoopilla |
2.2 Pohjusteen suunnittelun periaatteet
| Monistettu fragmentin koko | Mieluiten 100-150 bp |
| Pohjamaalin pituus | 18-25 bp |
| GC sisältö | 30-70 %, mieluiten 45-55 % |
| Tm-arvo | 58-60 ℃ |
| Järjestys | Vältä T/C jatkuvaa;A/G jatkuva |
| 3 loppujakso | Vältä GC-rikasta tai AT-rikasta;päätepohja on edullisesti G tai C;on parasta välttää T |
| Täydentävyys | Vältä komplementaarisia sekvenssejä, joissa on yli 3 emästä alukkeessa tai kahden alukkeen välillä |
| Spesifisyys | Käytä blast-hakua alukkeen spesifisyyden vahvistamiseksi |
①SiRNA on lajispesifinen ja eri lajien sekvenssit ovat erilaisia.
②SiRNA on pakattu pakastekuivattuun jauheeseen, jota voidaan säilyttää stabiilisti 2-4 viikkoa huoneenlämmössä.
2.3 Työkalut tai reagenssit, jotka on valmisteltava etukäteen
| Primer (sisäinen viite) | Sisältää kaksi eteen- ja taaksepäin |
| Alukkeet (kohdegeeni) | Sisältää kaksi eteen- ja taaksepäin |
| Kohde Si-RNA (3 liuskaa) | Yleensä yritys syntetisoi 3 nauhaa ja valitsee sitten yhden kolmesta RT-PCR:llä |
| Transfektiosarja | Lipo2000 jne. |
| RNA Rapid Extraction Kit | RNA:n uuttamiseen transfektion jälkeen |
| Rapid Reverse Transcription Kit | cDNA-synteesiä varten |
| PCR-amplifikaatiosarja | 2×Super SYBR vihreä qPCR Master Mix |
2.4 Mitä tulee seikkoihin, joihin on kiinnitettävä huomiota tietyissä kokeellisissa vaiheissa:
①siRNA-transfektioprosessi
1. Maljaukseen voit valita 24-kuoppaisen, 12-kuoppaisen tai 6-kuoppaisen levyn (24-kuoppaisen levyn kussakin kuoppassa ehdotettu keskimääräinen RNA-pitoisuus on noin 100-300 ng/uL), ja solujen optimaalinen transfektiotiheys on jopa 60-80 %.
2. Transfektiovaiheet ja erityisvaatimukset ovat tiukasti ohjeiden mukaisia.
3. Transfektion jälkeen näytteet voidaan kerätä 24-72 tunnin sisällä mRNA-detektioon (RT-PCR) tai proteiinien havaitsemiseen 48-96 tunnin sisällä (WB).
② RNA-uuttoprosessi
1. Estä ulkoisten entsyymien aiheuttama kontaminaatio.Se sisältää pääasiassa maskien ja käsineiden tiukan käytön;käyttämällä steriloituja pipetin kärkiä ja EP-putkia;kokeessa käytetyn veden on oltava RNaasi-vapaata.
2. On suositeltavaa tehdä kaksi kertaa pikauuttosarjassa ehdotetulla tavalla, mikä todella parantaa puhtautta ja saantoa.
3. Jäteneste ei saa koskettaa RNA-kolonnia.
③ RNA:n kvantifiointi
Kun RNA on uutettu, se voidaan määrittää suoraan Nanodropilla, ja vähimmäislukema voi olla niinkin alhainen kuin 10 ng/ul.
④Käänteinen transkriptioprosessi
1. RT-qPCR:n korkean herkkyyden vuoksi kullekin näytteelle tulisi tehdä vähintään 3 rinnakkaista kuoppaa, jotta myöhempi Ct ei olisi liian erilainen tai SD ei olisi liian suuri tilastollista analyysiä varten.
2. Älä jäädytä ja sulata Master mixiä toistuvasti.
3. Jokainen putki/reikä on korvattava uudella kärjellä!Älä käytä jatkuvasti samaa pipetin kärkeä näytteiden lisäämiseen!
4. Näytteen lisäämisen jälkeen 96-kuoppaiseen levyyn kiinnitetty kalvo on tasoitettava levyllä.On parasta sentrifugoida ennen sen asettamista koneelle, jotta putken seinämän neste pääsee valumaan alas ja poistamaan ilmakuplat.
⑤Yleinen käyräanalyysi
| Ei logaritmisen kasvujaksoa | Mahdollisesti korkea mallin pitoisuus |
| Ei CT-arvoa | Väärät vaiheet fluoresoivien signaalien havaitsemiseksi; alukkeiden tai koettimien hajoaminen – sen eheys voidaan havaita PAGE-elektroforeesilla; riittämätön määrä mallia; mallien hajoaminen – epäpuhtauksien ja toistuvan jäädytyksen ja sulatuksen välttäminen näytteen valmistelussa; |
| Ct>38 | Alhainen vahvistusteho;PCR-tuote on liian pitkä;erilaiset reaktiokomponentit hajoavat |
| Lineaarinen vahvistuskäyrä | Anturit voivat hajota osittain toistuvien jäädytys-sulatusjaksojen tai pitkittyneen valolle altistumisen seurauksena |
| Ero kaksoisrei'issä on erityisen suuri | Reaktioliuos ei ole täysin sulanut tai reaktioliuosta ei sekoiteta;PCR-laitteen lämpökylpy on fluoresoivien aineiden saastuttama |
2.5 Tietojen analysoinnista
QPCR:n data-analyysi voidaan jakaa suhteelliseen kvantifiointiin ja absoluuttiseen kvantifiointiin.Esimerkiksi hoitoryhmän solut verrattuna kontrolliryhmän soluihin,
Kuinka monta kertaa X-geenin mRNA muuttuu, tämä on suhteellinen kvantifiointi;tietyssä määrässä soluja X-geenin mRNA
Kuinka monta kopiota on, tämä on absoluuttinen määrä.Yleensä laboratoriossa käytämme eniten suhteellista kvantitatiivista menetelmää.Yleensä,2-ΔΔct-menetelmälläkäytetään eniten kokeissa , joten vain tämä menetelmä esitellään tässä yksityiskohtaisesti.
2-ΔΔct-menetelmä: Saatu tulos on ero kohdegeenin ilmentymisessä koeryhmässä verrattuna kohdegeeniin kontrolliryhmässä.Vaaditaan, että sekä kohdegeenin että sisäisen vertailugeenin monistustehokkuus on lähellä 100 % ja suhteellinen poikkeama ei saa ylittää 5 %.
Laskentamenetelmä on seuraava:
Δct kontrolliryhmä = kohdegeenin ct-arvo kontrolliryhmässä – sisäisen vertailugeenin ct-arvo kontrolliryhmässä
Δct koeryhmä = kohdegeenin ct-arvo koeryhmässä – sisäisen vertailugeenin ct-arvo koeryhmässä
ΔΔct = Δct kokeellinen ryhmä - Δct kontrolliryhmä
Lopuksi laske lauseketason eron kerrannainen:
Muuta Fold=2-ΔΔct (vastaa excel-funktiota POWER)
Liittyvät tuotteet:
Postitusaika: 20.5.2023