Epidemian alkuvaiheessa nopeasta kehityksestä johtuen epäiltyjen potilaiden nopea diagnoosi on avain COVID-19:n ehkäisyyn.Joillakin hyväksytyillä nukleiinihapon havaitsemisreagensseilla on lyhyt kehitysaika, ja niissä on ongelmia, kuten nopea suorituskyvyn vahvistus, riittämätön reagenssin optimointi ja suuret erot erien välillä;Erilaisten kliinisten laboratorioiden ongelmat nukleiinihapon havaitsemisprosessin eri osa-alueilla voivat myös vaikuttaa nukleiinihapon havaitsemistulosten tarkkuuteen.Tässä artikkelissa keskitytään tärkeimpiin linkkeihin ja kohtiin nykyisessä SARS-CoV-2-nukleiinihappojen havaitsemisessa ja analysoidaan laboratorionukleiinihappojen havaitsemisen väärien negatiivisten ja positiivisten uudelleentarkastelun ja kliinisen epäjohdonmukaisuuden ongelmia.
SARS-CoV-2-nukleiinihappojen havaitsemisen periaatteet
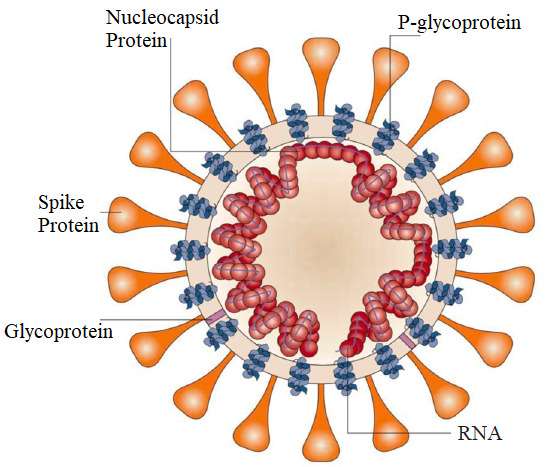
SARS-CoV-2 on RNA-virus, jonka genomisekvenssi on noin 29 kb ja 10 geeniä, jotka voivat tehokkaasti koodata 10 proteiinia.Virukset koostuvat RNA:sta ja proteiineista, ja uloin kerros on lipideistä ja glykoproteiineista koostuva ulkopäällyste.Sisällä proteiinikapsidi kääri RNA:n siihen ja suojaa siten helposti hajoavaa RNA:ta (P1).
P1 SARS-COV-2:n rakenne
Virukset tunkeutuvat soluihin tiettyjen solun pintareseptorien kautta aiheuttaen infektion ja käyttävät isäntäsoluja replikoitumiseen.
Viruksen nukleiinihapon havaitsemisen periaate on paljastaa viruksen RNA solulysaatin läpi ja käyttää sitten reaaliaikaista fluoresoivaa käänteistranskriptiopolymeraasiketjureaktiota (RT-PCR) havaitsemiseen.
Havaitsemisperiaatteen avain on käyttää alukkeita ja koettimia nukleiinihapposekvenssien "kohdennettuun yhteensovittamiseen" eli löytää SARS-CoV-2:n nukleiinihapposekvenssi, joka eroaa muista viruksista noin 30 000 emäksellä (nukleiinihapon samankaltaisuus muihin viruksiin) "matala"-alue, suunnittelu alukkeet ja koettimet.
Alukkeet ja koettimet sopivat hyvin yhteen SARS-CoV-2-nukleiinihapon spesifisen alueen kanssa, eli spesifisyys on erittäin vahva.Kun testattavan näytteen reaaliaikainen fluoresoiva RT-PCR-monistustulos on positiivinen, se osoittaa, että näytteessä on SARS-CoV-2:ta.Katso P2.
SARS-CoV-2-nukleiinihappomäärityksen P2-vaiheet (reaaliaikainen fluoresoiva RT-PCR)
Laboratorion olosuhteet ja vaatimukset SARS-CoV-2-nukleiinihappojen havaitsemiseksi
Nukleiinihappojen testauslaboratoriot ovat ihanteellisia alipaineympäristöihin, ja niissä tulee kiinnittää huomiota paineen seurantaan, pitää ilman virtaus ja eliminoida aerosolit.Nukleiinihappotestaushenkilöstöllä on oltava vastaava pätevyys, heillä on oltava asianmukainen polymeraasiketjureaktiokoulutus ja läpäistävä arviointi.Laboratoriota tulee hallita tiukasti, se on jaettava paikalleen, ja asiaankuulumattomien henkilöiden pääsy sisään on ehdottomasti kielletty.Puhdas alue on tuuletettava ja desinfioitava paikallaan.Asiaankuuluvat esineet sijoitetaan vyöhykkeille, puhtaat ja likaiset erotetaan, vaihdetaan ajoissa ja dekontaminoidaan paikoilleen.Säännöllinen desinfiointi: Klooripitoinen desinfiointiaine on pääratkaisu isommille alueille ja 75 % alkoholia voidaan käyttää pienille alueille.Hyvä tapa käsitellä aerosoleja on avata ikkunat tuuletusta varten, ja ilman desinfiointi voidaan tehdä myös ultraviolettisäteillä, suodatuksella ja ilman desinfioinnilla.
SARS-CoV-2-nukleiinihappomäärityksen keskeiset linkit ja parametrit (reaaliaikainen fluoresoiva RT-PCR)
Vaikka laboratoriot kiinnittävät yleensä erityistä huomiota nukleiinihappojen "detektioon", itse asiassa nukleiinihappojen "uutto" on myös yksi onnistuneen havaitsemisen avainvaiheista, mikä liittyy läheisesti virusnäytteiden keräämiseen ja säilytykseen.
Tällä hetkellä yleisimmin käytetyissä hengitysnäytteissä, kuten nenänielun vanupuikoissa, käytetään toista menetelmää, joka on nukleiinihappouuttoon ja lyysiliuokseen perustuva inaktivointi (säilöntä)liuos.Toisaalta tämä viruksen säilytysliuos voi denaturoida viruksen proteiinin, menettää aktiivisuutensa eikä olla enää tarttuva, ja parantaa kuljetus- ja havaitsemisvaiheen turvallisuutta;toisaalta se voi suoraan murtaa viruksen vapauttaakseen nukleiinihapon, eliminoidakseen nukleiinihappoa hajottavan entsyymin ja estääkseen viruksen.RNA hajoaa.
Virusnäytteenottoliuos, joka on valmistettu nukleiinihappouutto-lyysiliuoksen perusteella.Pääkomponentit ovat tasapainotetut suolat, etyleenidiamiinitetraetikkahappokelatointiaine, guanidiinisuola (guanidiini-isotiosyanaatti, guanidiinihydrokloridi jne.), anioninen pinta-aktiivinen aine (dodekaani) Natriumsulfaatti), kationinen pinta-aktiivinen aine (tetradekyylitrimetyyliammonium-K-oksalaatti, dihydroteenoksi-oksalaatti, dihydroteenoksi-oksalaatti8, p-, dihydroteenoksi-oksalaatti8). muita useita tai useampia komponentteja.Tällä hetkellä on olemassa monenlaisia nukleiinihappojen uuttopakkauksia, ja käytetään erilaisia nukleiinihappojen uutto- ja puhdistusreagensseja.Vaikka käytettäisiin samaa nukleiinihappouutto- ja puhdistusreagenssia, kunkin sarjan uuttomenetelmät ovat erilaisia.
Tällä hetkellä National Medical Products Administrationin hyväksymät nukleiinihappojen havaitsemispakkaustuotteet valitaan SARS-CoV-2-genomin ORF1ab-, E- ja N-geenien perusteella.Eri tuotteiden havaitsemisperiaatteet ovat periaatteessa samat, mutta niiden alukkeet ja anturimallit ovat erilaisia.On yhden kohdesegmentin (ORF1ab), kahden kohdesegmentin (ORF1ab, N tai E) ja kolmen kohdesegmentin (ORF1ab, N ja E) segmenttejä.Havaitsemisen ja tulkinnan, nukleiinihapon uuton ja reaaliaikaisen fluoresoivan RT-PCR-reaktiojärjestelmän väliset erot tulee viitata asiaankuuluviin pakkauksen ohjeisiin, ja on suositeltavaa, että käyttäjät noudattavat tarkasti pakkauksen tulkintaohjeissa määritettyä tulkintamenetelmää.Yhteiset alueet, alukkeet ja koetinsekvenssit, jotka on monistettu reaaliaikaisella fluoresoivalla RT-PCR:llä, on esitetty P3:ssa.
P3 SARS-CoV-2-amplikonin kohteen sijainti genomissa sekä alukkeiden ja koettimien sekvenssi
SARS-CoV-2-nukleiinihappomäärityksen tulosten tulkinta (Rsyö-Time fluoresoiva RT-PCR)
"Pneumonian ehkäisy- ja hallintasuunnitelma SARS-CoV-2-infektiolle (toinen painos)" selvensi ensimmäistä kertaa kriteerit yksittäisen geenin monistumisen tulosten arvioimiseksi:
1. Ei Ct tai Ct≥40 on negatiivinen;
2. Ct<37 on positiivinen;
3. Ct-arvo 37-40 on harmaasävyalue.On suositeltavaa toistaa koe.Jos Ct<40 uudelleenmäärityksen tuloksella ja vahvistuskäyrällä on ilmeisiä huippuja, näyte katsotaan positiiviseksi, muuten se on negatiivinen.
Oppaan kolmas painos ja oppaan neljäs painos jatkoivat edellä mainittuja kriteerejä.Kaupallisissa sarjoissa käytettävien erilaisten kohteiden vuoksi edellä mainitussa oppaan 3. painoksessa ei kuitenkaan annettu kriteerejä maalien yhdistelmän määrittämiselle, korostaen, että valmistajan antamia ohjeita sovelletaan.Ohjeen viidennestä painoksesta lähtien on selvennetty kahta tavoitetta, erityisesti yksittäisen vaikeasti arvioitavan kohteen arviointikriteerejä.Toisin sanoen, jos laboratorio haluaa varmistaa, että tapaus on positiivinen SARS-CoV-2-nukleiinihapon havaitsemiseksi, seuraavien on täytettävä yksi kahdesta ehdosta:
(1) Kaksi SARS-CoV-2-kohdetta (ORF1ab, N) samassa näytteessä testataan positiivisiksi reaaliaikaisella fluoresoivalla RT-PCR:llä.Jos yksittäinen tavoite on positiivinen, vaaditaan uusintanäytteenotto ja uusintatestaus.Jos testitulokset ovat Jos yksittäinen kohde on edelleen positiivinen, se katsotaan positiiviseksi.
(2) Kaksi reaaliaikaista fluoresoivaa RT-PCR-näytettä osoitti yhtä kohdepositiivista samaan aikaan tai kaksi samantyyppistä näytettä osoittivat yhden kohdepositiivisen testituloksen, joka voidaan katsoa positiiviseksi.Ohjeissa korostetaan kuitenkin myös sitä, että nukleiinihappotestien negatiiviset tulokset eivät voi sulkea pois SARS-CoV-2-infektiota.Tekijät, jotka voivat aiheuttaa vääriä negatiivisia tuloksia, on suljettava pois, mukaan lukien huono näytteen laatu (hengitysnäytteet suunielusta ja muista osista), näytteenotto liian aikaisin tai liian myöhään, näytteitä ei varastoitu, kuljetettu ja käsitelty oikein, ja itse tekniikassa oli ongelmia (viruksen vaihtelu, PCR:n esto) jne.
Väärien negatiivisten tulosten syyt SARS-CoV-2-tunnistuksessa
Käsite "väärä negatiivinen" tällä hetkellä kyseessä olevassa nukleiinihappotestauksessa viittaa usein "vääriin negatiivisiin", joissa nukleiinihappotestien tulokset ovat ristiriidassa kliinisten ilmenemismuotojen kanssa, eli kliinisiä oireita ja kuvantamistuloksia epäillään vahvasti COVID-19:stä, mutta nukleiinihappotestit ovat aina "negatiivisia" monta kertaa.Kansallisen terveyskomission kliininen laboratoriokeskus selitti "väärä negatiivisen" SARS-CoV-2-testin.
(1) Tartunnan saaneen henkilön soluissa on tietty määrä virusta.Olemassa olevat tiedot osoittavat, että kun keho on saanut viruksen tartunnan, virus pääsee kurkkuun nenän ja suun kautta, sitten henkitorveen ja keuhkoputkiin ja saavuttaa sitten keuhkorakkuloihin.Tartunnan saanut kokee itämisajan, lieviä oireita ja sitten vaikeiden oireiden prosessin ja taudin eri vaiheita.Ja viruksen määrä kehon eri osissa on erilainen.
Mitä tulee solutyyppien viruskuormitukseen, keuhkorakkuloiden epiteelisolut (alahengitystiet)> hengitysteiden epiteelisolut (ylempi hengitystiet)> fibroblastit, endoteelisolut ja makrofagit jne.;näytetyypistä alveolaarinen huuhteluneste (erinomaisin)>syvä yskivä yskös>nenänielun vanupuikko>suunnielun vanupuikko>veri.Lisäksi virus voidaan havaita myös ulosteista.Leikkauksen mukavuuden ja potilaiden vastaanoton vuoksi yleisesti käytetty kliininen näytejärjestys on kuitenkin suunielun vanupuikko>nenänielun vanupuikko> keuhkoputken huuhteluneste (monimutkainen leikkaus) ja syvä yskös (yleensä kuiva yskä, vaikea saada) .
Siksi joidenkin potilaiden suunielun tai nenänielun solujen virusmäärä on pieni tai erittäin alhainen.Jos testaukseen otetaan näytteitä vain suunielusta tai nenänielusta, viruksen nukleiinihappoa ei havaita.
(2) Viruksia sisältäviä soluja ei kerätty näytteenoton aikana tai virusnukleiinihappoa ei säilytetty tehokkaasti.
[① Väärä keräyspaikka, esimerkiksi suunielun vanupuikkoja otettaessa, keräyssyvyys ei ole riittävä, kerättyjä nenänielun vanupuikkoja ei kerätä syvälle nenäonteloon jne. Suurin osa kerätyistä soluista saattaa olla viruksettomia soluja;
② Näytteenottopuikkoja on käytetty väärin.Vanupuikkopään materiaaliksi suositellaan esimerkiksi synteettisiä kuituja, kuten PE-kuitua, polyesterikuitua ja polypropeenikuitua.Luonnonkuituja, kuten puuvillaa, käytetään varsinaisessa toiminnassa (voimakas proteiinin adsorptio ja ei helppo pestä pois) ja nailonkuituja (huono veden imeytyminen, mikä johtaa riittämättömään näytteenottomäärään);
③ Virusvarastoputkien virheellinen käyttö, kuten polypropeeni- tai polyeteenimuovisten säilytysputkien väärinkäyttö, jotka imevät helposti nukleiinihappoja (DNA/RNA), mikä johtaa nukleiinihapon pitoisuuden laskuun säilytysliuoksessa.Käytännössä virusnukleiinihappojen varastointiin suositellaan käytettäväksi polyeteeni-propeenipolymeerimuovia ja joitain erikoiskäsiteltyjä polypropeenimuovisäiliöitä.]
[① Väärä keräyspaikka, esimerkiksi suunielun vanupuikkoja otettaessa, keräyssyvyys ei ole riittävä, kerättyjä nenänielun vanupuikkoja ei kerätä syvälle nenäonteloon jne. Suurin osa kerätyistä soluista saattaa olla viruksettomia soluja;
② Näytteenottopuikkoja on käytetty väärin.Vanupuikkopään materiaaliksi suositellaan esimerkiksi synteettisiä kuituja, kuten PE-kuitua, polyesterikuitua ja polypropeenikuitua.Luonnonkuituja, kuten puuvillaa, käytetään varsinaisessa toiminnassa (voimakas proteiinin adsorptio ja ei helppo pestä pois) ja nailonkuituja (huono veden imeytyminen, mikä johtaa riittämättömään näytteenottomäärään);
③ Virusvarastoputkien virheellinen käyttö, kuten polypropeeni- tai polyeteenimuovisten säilytysputkien väärinkäyttö, jotka imevät helposti nukleiinihappoja (DNA/RNA), mikä johtaa nukleiinihapon pitoisuuden laskuun säilytysliuoksessa.Käytännössä virusnukleiinihappojen varastointiin suositellaan käytettäväksi polyeteeni-propeenipolymeerimuovia ja joitain erikoiskäsiteltyjä polypropeenimuovisäiliöitä.]
(4) Kliinisen laboratorion toimintaa ei ole standardoitu.Näytteiden kuljetus- ja säilytysolosuhteet, kliinisten laboratorioiden standardoitu toiminta, tulosten tulkinta ja laadunvalvonta ovat keskeisiä tekijöitä testitulosten tarkkuuden ja luotettavuuden varmistamiseksi.Kansallisen terveyslautakunnan kliinisen laboratoriokeskuksen 16.-24.3.2020 tekemän ulkoisen laatuarvioinnin tulosten mukaan 844:stä pätevän tuloksen saaneesta laboratoriosta 701 (83,1 %) oli päteviä ja 143 (16,9 %) ei.Pätevänä laboratorioiden yleiset testausolosuhteet ovat hyvät, mutta eri laboratorioissa on edelleen eroja henkilöstön toimintakyvyssä, yhden kohteen positiivisen näytteen tulkintakyvyssä ja laadunvalvonnassa.
Kuinka vähentää SARS-CoV-2-nukleiinihappotunnistuksen väärää negatiivista määrää?
Väärien negatiivisten tulosten vähentäminen nukleiinihappojen havaitsemisessa tulisi optimoida väärien negatiivisten tuottamisen neljän näkökohdan perusteella.
(1) Tartunnan saaneen henkilön soluissa on tietty määrä virusta.Viruksen pitoisuus tartunnan saaneiden henkilöiden kehon eri osissa on erilainen eri aikoina.Jos nielua ei ole, se voi olla keuhkoputkien huuhtelunesteessä tai ulosteessa.Jos usean tyyppisiä näytteitä voidaan kerätä samanaikaisesti tai taudin etenemisen eri vaiheissa testausta varten, auttaa välttämään vääriä negatiivisia tuloksia.
(2) Virusta sisältävät solut on kerättävä näytteenoton aikana.Tämä ongelma voidaan ratkaista suurelta osin vahvistamalla näytteenkeräjien koulutusta.
(3) Luotettavat IVD-reagenssit.Kansallisella tasolla tekemällä tutkimusta reagenssien havaitsemissuorituskyvyn arvioinnista ja keskustelemalla olemassa olevista ongelmista reagenssien havaitsemistehokkuutta voidaan edelleen parantaa ja analyysin herkkyyttä parantaa.
(4) Kliinisten laboratorioiden standardoitu toiminta.Laboratoriohenkilöstön koulutusta vahvistamalla, laboratorion laadunhallintajärjestelmää jatkuvasti parantamalla, kohtuullisia jakoja varmistamalla ja henkilöstön havaitsemiskykyä parantamalla voidaan vähentää virheellisestä laboratoriotoiminnasta johtuvia vääriä negatiivisia.
Syitä SARS-CoV-2-nukleiinihappotestin uusintapositiiviseen positiiviseen tulokseen toipuneilla ja kotiutuneilla potilailla
"COVID-19-diagnoosi- ja hoitosuunnitelma (Trial Seventh Edition)" määrää selvästi, että yksi kriteereistä COVID-19-potilaiden parantumiselle ja sairaalasta kotiuttamiselle on, että kahdessa peräkkäisessä hengitystienäytteessä on negatiivinen nukleiinihappotesti (vähintään 24 tunnin välein), mutta on hyvin vähän eri syitä.
(1)SARS-CoV-2 on uusi virus.On tarpeen ymmärtää tarkemmin sen patogeeninen mekanismi, täydellinen kuva aiheuttamasta taudista ja taudin kulun ominaisuudet.Siksi on toisaalta tarpeen vahvistaa kotiutuneiden potilaiden hoitoa ja suorittaa 14 päivän lääketieteellistä tarkkailua.Suorita seurantaa, terveyden seurantaa ja terveysohjausta syventääksesi ymmärrystä taudin esiintymisen, kehittymisen ja lopputuloksen koko prosessista.
(2) Potilas voi saada uudelleen viruksen tartunnan.Akateemikko Zhong Nanshan sanoi: Koska parantuneilla potilailla on vasta-aineita, SARS-CoV-2 voidaan eliminoida vasta-aineilla, kun ne hyökkäävät uudelleen.Syitä on monia, jotka voivat olla toipuneen potilaan syy tai se voi liittyä viruksen mutaatioon tai jopa laboratoriotutkimukseen.Jos kyseessä on itse virus, SARS-CoV-2-mutaatio voi saada toipuneen potilaan tuottaman vasta-aineen tehottomaksi mutatoitunutta virusta vastaan.Jos potilas saa mutatoituneen viruksen tartunnan uudelleen, nukleiinihappotesti voi olla jälleen positiivinen.
(3) Laboratoriotestimenetelmien osalta jokaisella testausmenetelmällä on rajoituksensa.SARS-CoV-2-nukleiinihapon havaitseminen johtuu geenisekvenssin valinnasta, reagenssien koostumuksesta, menetelmän herkkyydestä ja muista syistä, mikä johtaa siihen, että olemassa olevilla sarjoilla on omat alemmat havaitsemisrajansa.Hoidon jälkeen viruksen määrä elimistössä vähenee.Kun testattavan näytteen viruskuorma on alle havainnointirajan, "negatiivinen" tulos tulee näkyviin.Tämä tulos ei kuitenkaan tarkoita, että virus kehosta olisi kadonnut kokonaan.Virus voi olla hoidon lopettamisen jälkeen.Resurgence”, jatka kopioimista.Siksi on suositeltavaa tarkistaa kerran viikossa 2–4 viikon kuluessa kotiutuksen jälkeen.
(4) Nukleiinihappo on viruksen geneettinen materiaali.Virus kuolee potilaalle antiviraalisen hoidon jälkeen, mutta jäljellä olevat viruksen RNA-fragmentit säilyvät edelleen ihmiskehossa eivätkä poistu kokonaan elimistöstä.Joskus tietyissä olosuhteissa se voidaan säilyttää paremmin.Pitkään, ja tällä hetkellä nukleiinihappotesti on "lyhytaikainen" positiivinen.Potilaan toipumisajan pidentyessä, sen jälkeen kun kehossa olevat jäännös-RNA-fragmentit ovat vähitellen loppuneet, nukleiinihappotestin tulos voi muuttua negatiiviseksi.
(5) SARS-CoV-2:n nukleiinihappotestin tulos todistaa vain viruksen RNA:n olemassaolon tai puuttumisen, eikä se voi osoittaa viruksen aktiivisuutta ja sitä, onko virus tarttuva.On tarpeen todistaa, tuleeko potilas, jonka nukleiinihappotesti on jälleen positiivinen, jälleen tartuntalähde.On tarpeen suorittaa virusviljely kliinisistä näytteistä ja viljellä "elävää" virusta sen osoittamiseksi, että se on tarttuva.
Yhteenveto
Yhteenvetona voidaan todeta, että SARS-CoV-2-nukleiinihappotestin vääriä negatiivisia tuloksia, uudelleentestipositiivisia tuloksia ja muita kliinisten ilmenemismuotojen kanssa ristiriidassa olevia olosuhteita ei voida täysin välttää.Varsinaisessa seulonnassa ja testauksessa on suositeltavaa yhdistää kliiniset oireet, kuvantamistutkimukset (CT) ja kokeet Laboratoriotesti (nukleiinihappotesti + virusspesifinen vasta-ainetesti) tulokset kattavan diagnoosin saamiseksi, jotta vältytään diagnoosilta puuttumiselta ja virhediagnoosilta.Jos testitulosten havaitaan olevan selvästi ristiriidassa kliinisten ilmenemismuotojen kanssa, on suositeltavaa tehdä kattava analyysi koko testilinkistä (näytteenotto-, kierto- ja käsittelylinkit), jotta voidaan sulkea pois SARS-CoV-2-viruksen varhainen infektio, uusiutuva infektio tai yhdistettynä muihin hengitystievirusinfektioihin jne.Jos olosuhteet sallivat, on suositeltavaa ottaa herkempiä näytteitä, kuten ysköstä tai alveolaarista huuhtelunestettä, uudelleentutkimusta varten.
Liittyvät tuotteet:
SARS-CoV-2 Nukleiinihapon havaitsemispakkaus (Multiplex PCR -fluoresoiva koetinmenetelmä)
Postitusaika: 03.09.2021